 Реферат: Переработка ТПО** и ТБО после проведения сепарации ТБО по группам
Реферат: Переработка ТПО** и ТБО после проведения сепарации ТБО по группам
Экспериментально установлено ускорение процесса анаэробного разложения природных дробленых растительных остатков в 2,5-3 раза по времени при введении ферментов амилазы и уропепсина из животного организма по сравнению с процессом анаэробного разложения этих же природных материалов без внесения ферментов.
Итак, далее на другую площадку (на другую карту) для приготовления биомассы из промышленных отходов, содержащих только С-компонент (в основном) выгружается N-содержащий субстрат. В качестве такого субстрата может использоваться любой навоз. Перед приготовлением биомассы производится дробление исходных компонентов до размеров указанных ранее. Далее после проверки всех расчетов и при полном соблюдении соотношения С/N = 25/1-30/1 производится интенсивное перемешивание всех С- и N-содержащих компонентов, находящихся на первой и второй площадках (картах)1. Перемешивание производится бульдозером. Участки, которые нельзя перемешать техническими средствами перемешиваются вручную. Смешение компонентов производится до полной гомогенизации (однородности). Начало перемешивания и приготовление биомассы лучше всего производить или осенью в конце сентября, в октябре (при плюсовой погоде) или в середине апреля (тоже при плюсовой температуре).
Как показали исследования ряда авторов и наши исследования процесс биодеградации протекает по времени весьма различно и в значительной мере зависит от свойств N-субстрата. Нами рассматривались системы с использованием в качестве N-субстрата конского, свиного навоза, навоза кроликов и навоза птицы (кур). Нами были поставлены специальные эксперименты по проверке выше упомянутых основных параметров экологической биотехнологии, указанных в работе (6). Изучено было также влияние вида азотсодержащего компонента (навоза различных домашних животных) на процесс биодеградации и влияние изменения соотношения С/N на ход процесса. Исследовалось влияние размеров кучи с биомассой (длина, высота, ширина). Длина изменялась от 2 до 100 метров; высота от 1 до 4 м; ширина от 2 до 10 м. Экспериментально были подтверждены следующие параметры процесса:
1. Длина ряда биомассы практически не влияет на процесс биодеградации.
2. При низкой высоте (меньше 1,5 м) кучи биомассы происходит нарушение процесса аэрации (т.е. воздушного вентилирования). При низкой высоте (ниже 1,5 м) ряд биомассы быстро подсыхает. Происходит нарушение процесса биодеградации. Процесс затягивается по времени. Увеличивается, так называемый, кажущийся индукционный период ферментативного разложения субстратов. Такое изменение высоты кучи для восстановления нормального хода процессов требует дополнительного водного орошения, особенно в засушливый период и увлажнения массы. Обычный температурный режим биодеградации нарушается (15).
Температура биодеградации в низком компостном ряду не превышает, как правило +50°С. А это может вызвать неполную естественную стерилизацию патогенной микрофлоры (паразитических клеток Salmonella spp., Brucеlla abortas, Ascaris suum) и паразитической микрофауны, например, гельминтофауны. Это нами также было подтверждено экспериментально (15).
3. При большой высоте компостного ряда до 4 м происходит нарушение естественной аэрации и процесс разложения также затягивается, увеличивается содержание промежуточных низкомолекулярных веществ в биомассе, что также является недопустимым.
4. Были подтверждены параметры по ширине ряда.
В итоге были еще раз проверены основные параметры биодеградации биомассы по способу экологической биотехнологии. Кроме того было проведено влияние соотношения С/N, влияние аэрации и размера частиц на протекание всех процессов и на свойства готовой биомассы, на завершенность процессов биодеградации. Почему мы несколько раз обращаем внимание на соотношение C/N? Потому, что это главнейший показатель для всего процесса переработки данной категории природных отходов способом экологической биотехнологии в биомассу. Это соотношение C/N = 25/1-30/1 определяет, во-первых, нормальный ход протекания процесса биодеградации и, во-вторых, предопределяет нормальные показатели получаемой биомассы.
Установлены следующие сроки биодеградации для различных видов N-субстратов (так называемые сроки ферментации, они колеблются весьма существенно). Под сроками ферментации понимается время (срок) от момента смешения С- и N-компонентов2 до времени внесения готовой биомассы в почву. Для следующих видов навоза сроки ферментации таковы:
а) для свиного навоза - 12 месяцев;
б) для конского навоза - 5-6 месяцев;
в) для кроличьего навоза - 5-6 месяцев;
г) для птичьего навоза - 18-20 месяцев;
д) для овечьего и козьего навоза - 6-7 месяцев.
Следует обратить внимание, что во всех изложенных вариантах приготовления биомассы нами не вводились искусственно, дополнительно ферменты. Биодеградация органического материала, как описывалось ранее, всегда сопровождается потерей веса до 40% от общей массы.
Нами экспериментально было показано, что добавление биомассы в любую почву в любых разумных количествах практически безвредно, но если только в ней отсутствуют тяжелые металлы (Cd, Pb, Hg, Sn, Ag, Au, Cr, Zn, Cu, Ni). Тяжелые металлы, по данным Говориной и Виноградовой, обладают канцерогенными свойствами (т.е. вызывают злокачественные новообразования) и мутагенным действием (т.е. вызывающим вырождение и мутацию живого организма) (16). По данным Черных, чем более растворимы тяжелые металлы, тем сильнее их негативное воздействие на биологическую активность почвенного слоя (17). По данным этих авторов, тяжелые металлы снижают ферментативную активность почвы. Эти тяжелые металлы, как выяснилось, образуют очень стабильные комплексные химические соединения, конкурируют с микроэлементами почвы за естественные хелатообразователи. Косвенное влияние тяжелых металлов выражается в нарушении процессов с участием ферментов, приводящих в конечном итоге к их инактивации (17). Особенно опасен Cd, за содержанием и поведением которого нужно осуществлять постоянный контроль в системе фонового экологического мониторинга. Увеличение содержания Zn в почве снижает поступление Cd в растения. С целью иммобилизации Cd в почвах и предотвращения его поступления в высшие растения рекомендуется проводить операцию известкования почвы, лучше всего осенью во влажную почву до наступления заморозков так, чтобы Ca++ максимально мог проникнуть в почвенный слой.
Итак, о втором этапе работы по разработке способа экологической биотехнологии приготовления биомассы излагаются исследования, проведенные по искусственному дополнительному введению ферментов в субстрат, содержащий целлюлозное волокно (для всех видов отходов) СЭД и ХЦ и соответствующее количество N-содержащего компонента в различных комбинациях. В качестве комбинаций ферментов опробовались образцы, предложенные лабораторией углеводов Института биохимии им. А.Н. Баха (А.Н. Клесов, М.Л. Рабинович), о чем упоминалось ранее. Исходя из технико-экономических соображений был выбран комбинированный препарат отечественного производства - целловиридин (содержащий экзоглюкозидазу, эндоглюканазу, целлобиогидролазу, пектиназу). Целловиридин - препарат без наполнителя с активностью по ФБ а пределах 500-2 000 ед/ч. Было установлено оптимальное количество вводимого фермента - 0,001% от веса исходной биомассы.
Известно, что ферменты (энзимы) являются специфическими биокатализаторами, присутствующими во всех живых клетках.
Все ферменты подразделяются на две большие группы:
1. Однокомпонентные, состоящие исключительно из белка.
2. Двухкомпонентные, состоящие из белка и небелковой части, называемой активной группой.
Классификация ферментов дается в работе (18) и излагается ниже.
1 класс - Оксидоредуктазы - катализируют окислительно-восстановительные процессы;
2 класс - Трансферазы - катализируют перенос различных функциональных групп, например, метильной (-СН3), карбонильной (-СООН);
3 класс - Гидролазы - катализируют гидролитические реакции (гидролизирующие сложно-эфирные, гликозидные и т.д. связи);
4 класс - Лиазы - вызывают негидролитическое расщепление связей -С-С-; -С-О-; -С-N- (декарбоксилазы);
5 класс - Изомеразы - катализируют процессы изомеризации;
6 класс - Лигазы (синтетазы) - катализируют процессы соединения двух субстратов.
Скорость ферментативной реакции зависит от активности фермента, которая выражается в различных единицах. Старой общепринятой единицей активности фермента является стандартная единица Е. Е - это количество фермента, которое катализирует превращение 1 мкМ субстрата [S] в 1 мин. при оптимальных условиях для данного фермента (t°С; рН, [S]). По последнему международному соглашению 1 единица n-фермента есть такое количество фермента, которое в определенных условиях катализирует превращение субстрата [S] со скоростью 1 мол/с. Эта единица называется катал (1 кат=6·107 стандартных единиц). Удельная активность, есть число единиц активности фермента, приходящихся на 1 мг белка в ферментативном препарате (Е/мг). Удельную активность фермента рекомендуется выражать в кат/кг.
Порядок реакции при ферментативном катализе изменяется. При небольших концентрациях субстрата [S] протекает реакция первого порядка (v - скорость процесса; v пропорциональна [S], т.е. скорость процесса пропорциональна концентрации субстрата). При насыщенной концентрации субстрата [S] скорость v не зависит от этой концентрации. Такая реакция характерна для реакции нулевого порядка. При промежуточных концентрациях субстрата [S] мы наблюдаем реакцию смешанного порядка (20).
Перед дальнейшем рассмотрении нами ферментативно-каталитических процессов остановимся для правильного понимания на свойствах ферментов, как биокатализаторов.
Для ферментов, как и для других чисто химических катализаторов характерен ряд общих свойств:
1. Ферменты не входят в состав конечных продуктов реакции и выходят из реакции в первоначальном виде. Они не расходуются в процессе катализа.
2. Ферменты не могут возбудить реакций противоречащих законам термодинамики. Они ускоряют только те процессы, которые могут протекать без них.
3. Ферменты не смещают положение равновесия, а лишь ускоряют его достижение.
В то же время для ферментов характерны специфические свойства, отличающие их от чисто химических катализаторов, а именно:
1. Все ферменты являются белками по химическому строению;
2. По сравнению с химическими катализаторами эффективность биокатализаторов-ферментов выше (скорость протекания процесса при участии фермента на несколько порядков выше, чем при участии химических катализаторов);
3. Ферменты обладают в отличие от химических катализаторов узкой специфичностью и избирательностью действия на субстраты. Имеется в виду действие на те вещества, превращение которых они катализируют;
4. Свойства биокатализаторов-ферментов регулируются;
5. При ферментативных процессах в отличие от неферментативных наблюдаются очень незначительные побочные процессы. То есть для ферментативных процессов характерен почти 100% выход основного вещества - продукта реакции. Это последнее специфическое отличие очень значимо.
Практически все химико-технологические процессы протекающие под непосредственным руководством человека и под его контролем всегда дают побочные процессы. Все эти процессы ускоряются химическими катализаторами. Одним из ранее незамеченным побочным процессом и был синтез галоидсодержащих диоксинов (ДО) и диоксиноподобных веществ (ДПВ), которые как оказалось в дальнейшем являются химическим СПИДом нашего времени. Таким образом, невольно приходится констатировать, что все созданное человеком и его уровень знаний окружающего мира далек от познания абсолютной истины, далек от совершенства.
Человек, вторгаясь в природное равновесие может по своему незнанию этих законов природы нарушать гармонию закономерностей, которые существуют в природе и тем самым вредить всему живому на земле и в первую очередь себе, не замечая об этом особенно в начале.
Итак, для ферментативно-каталитического процесса справедливо уравнение Михаэлиса (19), а именно скорость процесса:
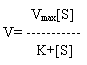
где К - константа Михаэлиса-Ментена: V=Vmax/2
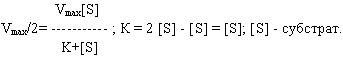
Теперь, после некоторого ознакомления с основными началами закономерностей ферментативных процессов вернемся конкретно к нашим системам. Знание этих закономерностей просто необходимо для дальнейшего изложения. Итак, процесс разложения полисахаридных отходов происходит под воздействием различных факторов, в т.ч. под влиянием фермента целлюлазы, который образуется анаэробными и аэробными бактериями. Общая схема ферментативно-каталитического разложения целлюлозно-бумажных и картонных отходов по Клесову - Рабиновичу приводится ниже (21),

| где |
Gn - исходный субстрат полисахарид-целлюлоза; |
|
Gn/x - нерастворимые продукты неупорядоченного гидролиза со значением степени полимеризации меньше, чем у исходной целлюлозы; |
|
|
G2 - целлобиоза; |
|
| G - глюкоза. |
Оптимум активности большинства грибных целлюлоз находится в слабокислой области, а именно рН=4,0-5,5. При этом некоторые ферменты сохраняют активность в более широком интервале рН. Ферменты из А.niger стабильны при 25°С в интервале рН=1-9 (21). Температурный оптимум активности целлюлолитических ферментов, продуцируемых мезофильными микроорганизмами находится в области +45-+55°С, термофильными +55-+70°С. Большинство грибных целлюлоз инактивируются при более высокой температуре и теряют всю каталитическую активность при +75-+80°С за несколько минут. Следует отметить, что для целлюлозно-бумажных и картонных отходов воздействие микроорганизмов проявляется, очевидно, в клеточной иммобилизации (а именно по методу внедрения (см. рис.8)) в субстрат.
Рис. 8. Вид клеточной иммобилизации (внедрение). Результаты биостарения твердых отходов производства целлюлозосодержащих материалов являются типичными для всех отходов содержащих целлюлозное волокно (18). Разберем поподробнее процессы биостарения таких материалов:
1. При введении целловиридина, как комбинированного целлюлолитического комплекса в ЦБО при биостарении образуется ряд органических продуктов в частности уксусный альдегид (ацетильдегид), который постепенно окисляется до уксусной кислоты АсОН. Оба вещества были нами обнаружены хроматографически благодаря Н.А. Беловой, которой мы выражаем сердечную благодарность (18). Одновременно происходит снижение рН от нейтрального значения до слабокислой реакции рН=4,5-4,0. В случае большого содержания влаги в субстрате это влияние уксусной кислоты весьма ощутимо. Влага, снижая доступ воздуха к субстрату и в частности кислорода, тем самым снижает возможность роста и развития аэробных бактерий и увеличивается возможность развития анаэробных, которые и вызывают существенное уже ощутимое и определяемое хроматографически появление уксусной кислоты в системе и ее влияние на рН субстрата.
2. Анализ полученных данных, приводимых в таблице 5.1 говорит о том, что процесс биологического разложения ЦБО является не только ферментативно-каталитическим, но и ферментативно-автокаталитическим, последовательным, сложным процессом с определенным периодом индукции, различным для различных субстратов и для различных концентраций фермента (см. таблицу 5.1).


