 Курсовая работа: Блистающий мир белков и пептидов
Курсовая работа: Блистающий мир белков и пептидов
Курсовая работа: Блистающий мир белков и пептидов
А.А. Замятнин, докт. биол. наук,
Институт биохимии им. А.Н. Баха РАН
Среди множества веществ, содержащихся в живом организме, особое место занимают белки. Их доля от сухой массы клеток млекопитающих составляет 60% – больше, чем для всех остальных вместе взятых химических соединений, и почти пятую часть от общей массы этих клеток. Каждый из сотен тысяч разных белков обладает уникальной химической и пространственной структурой, которые определяют его специфические функции.
Систематическое исследование структуры и функций многочисленных белков и их природных фрагментов – олигопептидов – началось во второй половине XX в. и продолжает стремительно развиваться. Каждый год публикуется несколько десятков тысяч научных работ, посвященных белковым веществам, многие тысячи ученых из более чем 50 стран ежедневно работают над этой проблемой. В последние годы сформировалась даже специальная наука протеомика, посвященная именно белкам. Не перестаешь восхищаться многообразию все новых и новых химических, структурных и функциональных форм белков, их взаимосвязи в осуществлении жизненно важных процессов, сложности и одновременно простоте всего этого, а также красоте как отдельных молекул, так и процессов с их участием. Белки и пептиды представляют собой удивительный и уникальный мир, для изучения которого необходимо привлечение знаний всех естественных, и не только естественных, наук. Именно с позиций разных наук и профессий мы и попытаемся заглянуть в этот блистающий мир человеческого знания.
Философия
На белки философы обратили внимание сразу же после того, как была выяснена их распространенность в живой природе и многообразие функций. И это неудивительно, поскольку по одному из определений философия – это наука о всеобщих законах развития природы, общества и мышления.
Широкое распространение получило определение жизни, данное Ф.Энгельсом в его труде «Анти-Дюринг», впервые полностью опубликованном в 1878 г. Обычно цитируют только первую часть этого определения. Приведем его полностью: «Жизнь есть способ существования белковых тел, и этот способ существования состоит по своему существу в постоянном самообновлении химических составных частей этих тел». В наши дни, когда о жизненно важных веществах и процессах известно неизмеримо больше, такое определение не может не вызывать ощущение неполноты и ограниченности. Однако и сам автор определения осознавал его уязвимость, написав в той же книге двумя страницами ниже: «Наше определение жизни, разумеется, весьма недостаточно, поскольку оно далеко от того, чтобы охватить все явления жизни, а, напротив, ограничивается самыми общими и самыми простыми среди них...»
По-видимому, Ф.Энгельс был первым из крупных философов, отметивших важность белков в жизнедеятельности организмов. По мере накопления новых биологических знаний эта тема постоянно остается предметом обсуждения и острых споров. Например, в 1969 г. автору этих строк довелось быть свидетелем дискуссии между двумя почтенными академиками – В.А. Энгельгардтом (1894–1984) и М.Н. Ливановым (1907–1986) о том, какие вещества – белки или нуклеиновые кислоты – являются определяющими в процессах памяти. Биохимик и физиолог затронули не только биологическую, но и философскую тему, поскольку память является неотъемлемой частью человеческого мышления, а мышление, как отмечено выше, – одна из философских проблем, составляющих ее определение как науки.
Очевидно, что все более глубокое философское осознание сущности живого и роли белков в жизнедеятельности будет происходить и в дальнейшем, но для этого необходимо исчерпывающе представлять себе всю проблему белков и пептидов, начиная с ее основ, которые мы и намереваемся обсудить.
Химия
Часто говорят, что белки состоят (образованы) из аминокислот. Несмотря на то что смысл этого утверждения прост и многим понятен, химик может отметить, что оно некорректно. Почему?
Да, действительно, в образовании белков участвуют аминокислоты. Однако при соединении друг с другом они перестают быть таковыми с химической точки зрения. Рассмотрим этот процесс более детально.
В живых организмах открыто несколько сотен различных аминокислотных структур, и все они могут быть охарактеризованы одной общей химической формулой в двух вариантах:
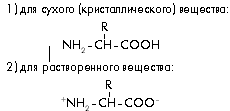
Во всех аминокислотах имеются аминная –NH3+ (N-конец) и карбоксильная –COO– (С-конец) группы, которые определяют соответственно основные и кислотные проявления этих веществ, в результате чего они обладают амфотерными (как щелочными, так и кислотными) свойствами.
Из приведенных формул также видно, что все эти вещества различаются лишь радикалами R. В образовании белков участвует 20 так называемых стандартных аминокислот, т.е. 20 различных радикалов R (табл. 1). Не обсуждая подробно химические особенности каждого радикала, отметив их лишь разными числовыми индексами i (R i), посмотрим, что произойдет с аминокислотами после соединения друг с другом.
Следующая формула характеризует вещество (трипептид) – результат соединения трех аминокислот (в растворе):
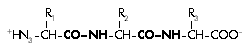
Присоединение 1-й аминокислоты ко 2-й и 2-й к 3-й сопровождается суммарным отщеплением двух молекул воды с образованием связей CO–NH, выделенных в формуле жирным шрифтом. Эта связь является ковалентной (сильной), называется пептидной, и ее название послужило основой для того, чтобы все вещества, устроенные подобным образом, называть пептидами (белки тоже являются пептидами) вне зависимости от того, сколько аминокислот участвовало в их образовании.
Таким образом, от второй аминокислоты, характеризующейся радикалом R2, остался лишь фрагмент:
![]()
Он называется аминокислотным остатком. Все аминокислотные остатки, расположенные не на концах большой пептидной цепи, характеризуются данной формулой, а концевые, очевидно, тоже не совсем аминокислоты, а остатки, хотя и несколько иные. С точки зрения химика корректно говорить, что белки состоят не из аминокислот, а из аминокислотных остатков. Поэтому общая химическая формула любого белка (пептида), состоящего из n аминокислотных остатков, должна быть записана как:
![]()
Приведенная формула свидетельствует о том, что в простейшей записи любой белок представляет собой линейную последовательность аминокислотных остатков, в которой есть остов (как бы скелет) с регулярно повторяющейся последовательностью радикалов –NH–CH–CO– и выступающие из этого остова боковые радикалы. Такая запись характеризует первичную структуру белка.
Последовательность аминокислотных остатков принято рассматривать в одном определенном направлении – от N- к С-концу. В связи с расшифровкой огромного количества природных аминокислотных последовательностей, а также в целях экономии места и ресурсов вычислительной техники в настоящее время принято пользоваться однобуквенной (латинской) записью аминокислотных остатков (однобуквенный аминокислотный код). В табл. 1 приведены не только общепринятые обозначения аминокислотных остатков, но также показано, какие существенные физико-химические особенности их отличают. Многообразие этих свойств лежит в основе способности каждой индивидуальной аминокислотной последовательности принимать свою, уникальную пространственную конфигурацию, и так же, как и аминокислоты, практически всегда быть амфотерным веществом.
Рассмотрение белков и пептидов с позиций химии будет неполным, если не отметить то, что иногда после синтеза белка на рибосоме (трансляции) происходит химическая модификация некоторых аминокислотных остатков (посттрансляционная модификация). В результате, например, остатки пролина и лизина могут превращаться в остатки оксипролина и оксилизина, к тирозильному остатку порой присоединяется сульфатная группа и т.д. Этот процесс приводит к тому, что в организме одновременно сосуществуют белки или пептиды с модифицированными и немодифицированными остатками. Так, пептид гастрин может быть сульфатирован и несульфатирован по одному из остатков тирозина, и, что очень важно в проявлении физиологических функций, сульфатированный гастрин существенно более активен.
Русский, English, Deutsch…
Слово белок появилось в русском языке задолго до того, как была выяснена химическая природа этого вещества. Этот термин представляет собой производное от прилагательного «белый» и служит характеристикой различий двух разных по цвету основных компонентов куриного яйца (белка и желтка). Синонимом белка является слово «протеин» (англ. protein), которое используется во всей научной (и не только научной) литературе и происходит от греческого слова prwto – прото (первый, главный, важнейший), чем с давних времен подчеркивалась его исключительная роль. А латинское слово белок – albumen (или albuminis), альбумин используется для целой группы уже давно известных белков.
Другое ключевое слово – пептид – происходит от греческого пепто (варить, переваривать) и отражает процесс расщепления длинных белковых молекул, в результате чего образуются короткие фрагменты. Однако, как уже было отмечено, с позиций химии, пептидами являются все белки. Поэтому для разделения коротких и длинных пептидных цепей в качестве приставок используются два других греческих слова: Хligoj –олигос (немногий, малый) и приставка polЪ – поли- (много, многое). В результате олигопептидами (или часто для краткости – пептидами) называют сравнительно короткие аминокислотные последовательности, а полипептидами (белками) – длинные. В дальнейшем мы часто будем пользоваться терминами белок и пептид, учитывая указанное различие.
Названия белков и пептидов очень разнообразны. Первоначально они давались в то время, когда их химическая (первичная) структура была еще неизвестна. Целым группам белков присваивались названия на основании того, как они растворяются в воде, в растворах нейтральных солей, щелочах, кислотах и органических растворителях (например, протамины). Однако затем наибольшее число названий конкретных веществ пептидной природы стало даваться по названию органа, ткани или целого животного, из которого они были выделены, и по функциям, которые они осуществляют.

Первый олигопептид был получен из мясного фарша и поэтому назван карнозином (от лат. carnis – мясо), название одного из основных белков мяса – миозин – произошло от соответствующего греческого слова мышца (mаj – миос), а целая группа белков гистонов получила название от греческого слова (istТ – хистос), характеризующего понятие ткань. Примером использования названия животного служит ксенопсин, выделенный из африканской гладкой шпорцевой лягушки Xenopus laevis. Функциональные свойства олигопептидов отражены, например, в названиях брадикининов и тахикининов, вызывающих, в частности, ослабление (брадикардию) и усиление (тахикардия) сердечной деятельности. Некоторые названия хранят в себе название места, где они были открыты: ригин – в г. Рига (Латвия), а тафтцин – в Тафтском университете (США). Можно долго рассказывать об этой стороне предмета, поскольку число подобных примеров исчисляется тысячами. Однако предоставим это занятие профессиональным историкам науки для всестороннего и полного исследования, тем более что такие работы уже ведутся. Приведем только один пример.
В 30-е гг. прошлого века в Германии из сыворотки крови лошади было выделено вещество, которому присвоили название субстанция P (P – латинское). В то время еще не умели определять химическую структуру достаточно больших пептидов, однако было ясно, что соединение относится к этому классу веществ. Через многие годы, когда автора работы уже не было в живых, встал вопрос: а почему вещество названо именно так? В результате появилось три гипотезы, ни одна из которых до сих пор однозначно не обоснована. Первая из них очевидна – получен белок, и в названии использована первая буква от английского слова protein. Вторая основана на том, что вещество было получено в виде порошка, а это английское слово (pouder) также начинается с буквы «P». И, наконец, третья обращена к родному языку автора, на этом языке (немецком) животное, из которого выделено вещество (лошадь), пишется как das Pferd.
Белки и пептиды изучают чуть ли не во всех странах, а в научных публикациях на эту тему используются языки многих народов мира. Если в начале истории изучения этих веществ большинство научных работ считалось престижным писать на французском или немецком, то примерно с середины прошлого века стало традицией публиковать работу с новыми принципиальными результатами наряду с родным языком также и на английском.
Элементарная математика и информатика
Удивительная простота изначальной (первичной) структуры белков и олигопептидов позволяет провести простой математический анализ всей совокупности этих веществ. Сначала зададимся вопросом: сколько существует разных линейных последовательностей, в написании которых может быть использовано 20 стандартных аминокислотных остатков? Если через N обозначить число возможных последовательностей, а через n – количество аминокислотных остатков в молекуле, то ответ на поставленный вопрос даст простейшая алгебраическая формула, учитывающая все возможные повторы аминокислотных остатков в одной структуре:
N = 20n.
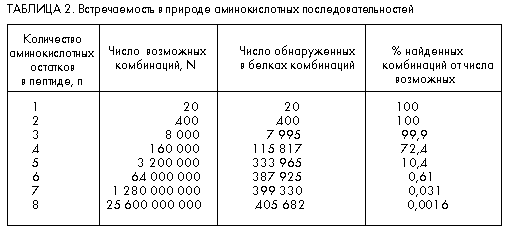
Из этой формулы следует, что максимальное число разных дипептидов (n = 2) равно 400, трипептидов (n = 3) – 8000, тетрапептидов (n = 4) – 160 000 и т.д. Как видим (см. табл. 2), число N очень быстро растет с увеличением n.
Тогда возникает другой вопрос: а каковы возможности живого организма вмещать в себя подобную информацию? Первичная информация содержится в нуклеотидной последовательности, и хотя она и очень велика, но все же не беспредельна. В табл. 3 представлены числа азотистых оснований суммарной ДНК у представителей разных царств живой природы. Первое, на что обращаешь внимание, это то, что общее их число варьирует в очень широких пределах и может составлять от 107 (некоторые бактерии и грибы) до 1011 (представители растений и рыб). При этом заметим, что царь природы человек отнюдь не является чемпионом среди других представителей живой природы, довольствуясь лишь примерно одним миллиардом азотистых оснований. Но для нас главное не это. Оказывается, самый большой геном не может вместить информацию даже о всех возможных декапептидах (n = 10) при их последовательном расположении.
Действительно, при n = 10:
N = 6,7х1011.
Eсли учесть то, что для записи одного аминокислотного остатка требуется 3 азотистых основания и что часть генома, шифрующая аминокислотные последовательности, составляет только несколько процентов от его общей величины, то получается, что самый большой геном способен вместить информацию о последовательности, состоящей лишь из 109 аминокислотных остатков. Таким образом, в нем может содержаться информация менее чем об 1% всех возможных декапептидов. А ведь известны белки, содержащие более 5 тыс. аминокислотных остатков!

Отсюда следует вывод о том, что в природе встречаются далеко не все линейные комбинации аминокислотных остатков. Это подтверждается компьютерным анализом встречаемости различных линейных комбинаций аминокислотных остатков во всех расшифрованных белках и пептидах (более 100 тыс.). Полученные результаты приведены в табл. 2, данные которой свидетельствуют о том, что в случае уже октапептидов (N = 8) встречается всего лишь около 0,001% возможных линейных комбинаций аминокислотных остатков.
А способна ли математика ответить на вопрос, решенный лингвистикой: можно ли дать строгое определение разницы между малыми и большими пептидами (олигопептидами и полипептидами)?
Попробуем на него ответить, пользуясь рассуждениями нашего великого соотечественника математика Андрея Николаевича Колмогорова (1903–1987), о малых (S) и больших (G) числах, свидетелем которых автор был на семинаре в МГУ в 1958 г. Колмогоров рассуждал примерно так. Числа существуют в определенной системе счисления. Система счисления, которой пользуется подавляющая часть человечества, определяется величиной m = 10. Тогда в рамках этой десятичной системы малыми числами будут такие, которые удовлетворяют условию m > S > m, а большие – G >> m. Иными словами, малые числа по порядку величины сравнимы с величиной основания системы счисления, а большие – во много раз ее больше.


